線粒體抵御帕金森氏癥的“質控”機制
日前,來自加拿大蒙特利爾神經學研究所的科學家們發現,與遺傳性帕金森氏癥相關的兩個基因參與了線粒體早期階段的質量控制。該保護機制可將氧化應激造成的受損蛋白從線粒體中移除。相關研究論文刊登在了近期出版的《歐洲分子生物學學會雜志》上。
論文資深作者 Edward Fon 教授表示,在細胞器內發生過度氧化損傷條件下,PINK1 和 parkin 基因可選擇性地將線粒體的功能失調組件導入溶酶體。研究揭示了這樣一種質量控制機制,即囊泡在線粒體中出芽,并繼續到溶酶體中退化。這種方法與之前已知的整個受損的線粒體的退化路徑有所不同。這是按照一個以小時計而不是以天計的時間表作出的提前反應。
這種退化機制旨在維持線粒體在整個細胞壽命期的完整性和功能性,被認為是包括帕金森氏癥在內的某些神經變性疾病的發展基礎。線粒體這個為細胞提供能量的“發電廠”發生故障就會導致帕金森氏癥。線粒體想要生存和發揮功能,就必須讓氧化受損的蛋白降解。
在該項研究中,研究人員使用免疫熒光和共聚焦顯微鏡來觀察囊泡如何從帶有受損負載的線粒體中被剪除。研究發現,PINK1 和 parkin 基因——從屬運輸系統的受損,可損害線粒體選擇性降解氧化受損蛋白質的能力。隨著時間的推移,就會導致在遺傳性帕金森氏癥中觀察到的線粒體功能障礙。
這兩種補救途徑都在細胞內運行。如果作為防御第一線的囊泡路徑被壓制,且損害不可逆,那么接下來整個細胞器將成為退化的目標。
本站所注明來源為"愛愛醫"的文章,版權歸作者與本站共同所有,非經授權不得轉載。
本站所有轉載文章系出于傳遞更多信息之目的,且明確注明來源和作者,不希望被轉載的媒體或個人可與我們
聯系zlzs@120.net,我們將立即進行刪除處理
熱點圖文
-
細數20年間卒中二級預防進展歷程
讓我們首先從抗血小板療法來進行討論。毫無疑問的是,阿司匹林對于卒中的二級預...[詳細]
-
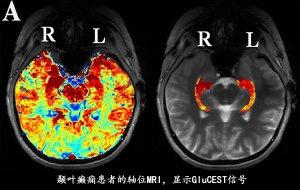
新型MRI成像技術可有效檢出癲癇病灶
研究者正在嘗試使用一種有力的影像學檢查工具,對難以尋覓的癲癇病灶進行定位。...[詳細]