廣泛期小細胞肺癌患者的長生存之路
基本病史
患者,女性,71歲,因“咳嗽、喘憋1周,發現右肺占位3天”于2020年9月24日入住腫瘤科。2020年9月17日患者在無明顯誘因下出現間斷咳嗽,干咳為主,活動耐量較前下降,走200米即出現喘憋。行X線胸片檢查提示“右肺門高密度影”。患2型糖尿病,口服降糖藥,血糖控制穩定;冠心病病史5年,曾行經皮冠狀動脈介入治療(PCI)。目前無胸悶、胸痛發作。吸煙40余年,約10支/天
入院檢查
入院后行血常規、肝功能、腎功能、電解質、空腹血糖等檢測,均基本正常;ProGRP420.44ng/L,神經元特異性烯醇化酶(NSE)93.45ug/L;2020年9月26日胸部CT檢查示(圖1):右肺下葉脊柱旁軟組織影,考慮右下肺中央型肺癌,伴右下肺不張改變;右肺門及縱隔內多發性腫大淋巴結。2020年9月27日支氣管鏡檢查示:右肺上葉開口清晰:右肺中葉開口輕度腫脹、尚光滑;右肺下葉開口充血,外壓飽滿,背段開口浸潤樣閉塞,咬取活檢質脆、易出血:左肺支氣管樹黏膜光滑,各葉段開口清晰,未見明確異常。病理診斷:(右肺下葉咬取活檢)小細胞癌,Ki-67(90%+),CK(+), TTF1(+),Syn(+), CgA(+), CD56(+)。2020年9月30日PET/CT檢查示:右肺下葉背段支氣管閉塞伴軟組織腫塊(約5.5cm×3.2cm,SUV值8.6);縱隔內氣管右后、腔靜脈周圍、主肺窗、隆突下及右肺門多發性結節及腫塊;第4胸椎、第1腰椎、右側髂骨及骶骨骨密度欠均,PET顯像可見放射性濃聚,考慮骨轉移。
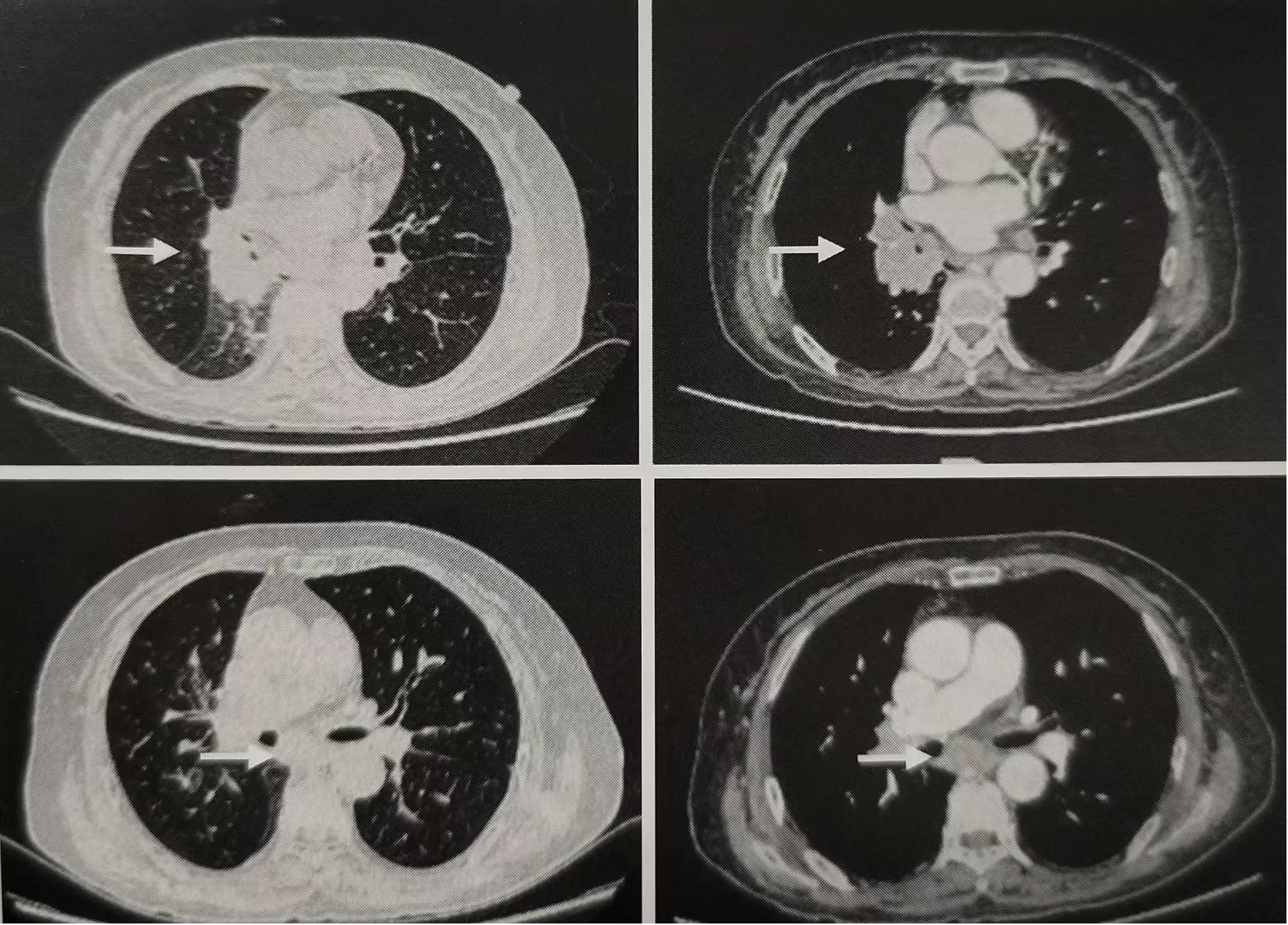
治療經過
患者目前診斷:右肺下葉小細胞癌廣泛期(ES-SCLC);冠心病PCI術后,心功能Ⅱ級(NYHA);2型糖尿病。
2020年10月9日起給予度伐利尤單抗1500mgd1+依托泊苷148mgd1-3+卡鉑300mgd1,4周期;12月17日起胸部調強放療45Gy/15次,其后度伐利尤單抗1500mgd1+依托泊苷148mgd1-3+卡鉑300mgd1,1周期;隨后度伐利尤單抗1500mg,維持4周期。
2021年2月療效評價近臨床完全緩解(nCR)。治療期間先后出現免疫相關性肺炎、放射性肺炎和放射性食管炎,給予積極對癥處理后明顯改善。
2021年12月隨訪PET/CT見右肺中葉局部復發,予以依托泊苷148mgd1-3+卡鉑300mgd1,4周期化療后病灶再次CR。其后患者規律復查CT及骨掃描,病情穩定,但時有吞咽困難,內鏡顯示食管中度狹窄,考慮與放療相關。
2022年5月行內鏡下綜合治療后管腔通暢,患者吞咽困難明顯改善。后規律復查隨訪,
2023年5月復查PET/CT示病灶穩定,接近CR。
末次隨訪為2024年10月20日,患者于2024年10月20日復查PET/CT提示第2、3胸椎周圍軟組織影,考慮骨轉移,相應水平脊髓不除外受累,正在進行局部放療。患者的OS>48個月。
臨床特征歸納
(1)患者,女性,71歲,因“咳嗽、喘憋1周,發現右肺占位3天”就診。既往有長期吸煙史。
(2)胸部CT檢查發現右肺下葉中央型肺癌,伴右肺門及縱隔淋巴結轉移。病理確診ES-SCLC。
(3)4周期度伐利尤單抗十依托泊苷十卡鉑(CE方案)治療,聯合胸部調強放療,最佳療效PR;其后免疫單藥維持4周期,療效nCR;半年后局部復發,PFS14個月。重啟CE方案4周期后病灶消失,病情持續緩解,PS32個月。OS>48個月。
(4)治療期間先后出現免疫相關性肺炎、放射性肺炎和放射性食管炎,經對癥處理后明顯改善。
治療過程討論
小細胞肺癌(SCLC)是一種難治、預后極差的肺癌亞型,其特征是快速生長和早期擴散,2020年CSC0肺癌指南標準線方案為鉑類聯合依托泊苷,PFS<6個月,0S 8-10個月,如何延長SCLC患者的生存期,是腫瘤科醫生面臨的挑戰。
一線選擇免疫聯合化療
本例患者2020年9月確診ES-SCLC,在當時免疫聯合化療方案剛進入NCCN指南一線治療,而PD-LI抑制劑阿替利珠單抗在我國尚未上市,患者及家屬積極治療的意愿非常強烈,結合當時CASPIAN研究結果[1],與家屬充分溝通后,最后給予度伐利尤單抗+依托泊苷+卡鉑治療。鑒于患者年齡大,體質偏弱,合并骨轉移,骨髓功能較差,AUC取4,給予“度伐利尤單抗1500mgd1+依托泊苷148mgd1-3+卡鉑300mgd1”方案。首次治療后患者咳嗽、喘憋緩解,2周期后影像學評價療效顯著,右肺門及縱隔腫塊明顯縮小,接近CR。
放療聯合免疫協同增效
2020年指南推薦,針對ES-SCLC患者,在療效判定CR或PR時,加用胸部放療可降低局部復發風險[2],然而這種放療指南推薦是基于免疫治療前時代,免疫治療加入后的可行性及安全性有待探索。考慮到放療聯合免疫治療可能有協同促進作用[3,4],能夠提高局部和全身控制率,獲得更長生存,降低復發風險,且該聯合的相關損傷風險均在可控范圍,結合患者意愿,我們最后采取了夾心療法(在第3周期治療結束,加入胸部調強放療45Gy),同時考慮到免疫治療聯合放療的潛在風險,在放療前后1個月,暫停全身洽療。治療過程順利,患者經過4周期同步放療、化療和免疫治療后病灶穩定,后續繼續給予4周期免疫單藥維持后,患者出現3級放射性肺炎和2級放射性食管炎,但均在臨床可控范圍,給予對癥支持治療后癥狀好轉。因考慮免疫相關性肺炎再燃風險,暫停免疫治療。
患者半年后局部復發,重啟CE方案,4周期后病灶消失。2023年5月復查PET/CT病灶接近CR。另外,對放射性食管炎進行了內鏡下綜合治療,患者的生活質量也得到明顯改善,PFS長達32個月。從發病到末次隨訪,患者已經獲得了超過4年的長生存,對于ES-SCLC患者來說,這是一個值得欣喜的結果。
總結
我們認為,早期的免疫聯合治療在這位患者中起到關鍵作用,同時局部放療的適時介入,也在患者生存上有明顯助力。當然不可否認的是,放療的介入可能增加放射性損傷風險,在免疫治療時代,這個問題也會越來越普遍。在本病例中,患者放療的時機比較激進,后續出現的放射性肺炎及食管炎,是否與放療聯合免疫治療相關,需持謹慎態度。如何選擇放療的介入時機,在延長生存的同時盡可能減少不良反應,也是我們臨床重點關注的問題。
參考文獻
1.PAZ-ARES L.DVORKIN M.CHEN Y,et al.Durvalumab plusplatinum-etoposide versus platinum-etoposide in first-line treatment ofextensive-stage small-cell lung cancer (CASPIAN):a randomized,controlled,open-label,phase 3 trial.Lancet,2019,394(10212):1929-1939.
2.YEE D.BUTTS C,REIMAN A,et al.Clinical trial of post-chemotherapy consolidation thoracic radiotherapy for extensive-stagesmall cell lung cancer].Radiother Oncol,2012,102(2):234-238.
3.WEICHSELBAUM RR,LIANG H,DENG L,et al.Radiotherapyand immunotherapy:a beneficial liaison [J]?Nat Rev Clin Oncol,2017,14(6):365-379.
4.WANG S J,HAFFTY B.Radiotherapy as a new player in immuno oncology.Cancers (Basel),2018,10(12):515.
本站所注明來源為"愛愛醫"的文章,版權歸作者與本站共同所有,非經授權不得轉載。
本站所有轉載文章系出于傳遞更多信息之目的,且明確注明來源和作者,不希望被轉載的媒體或個人可與我們
聯系zlzs@120.net,我們將立即進行刪除處理
熱點圖文
-
多參數MRI在前列腺癌精準診斷應用思考
隨著前列腺癌發病率的逐年上升,精準診斷與分層治療成為改善患者預后的關鍵。多...[詳細]
-
帶狀皰疹神經疼痛的臨床診療
綜合治療的必要性帶狀皰疹神經痛的治療需要多模式、多學科的綜合治療策略。結合...[詳細]

